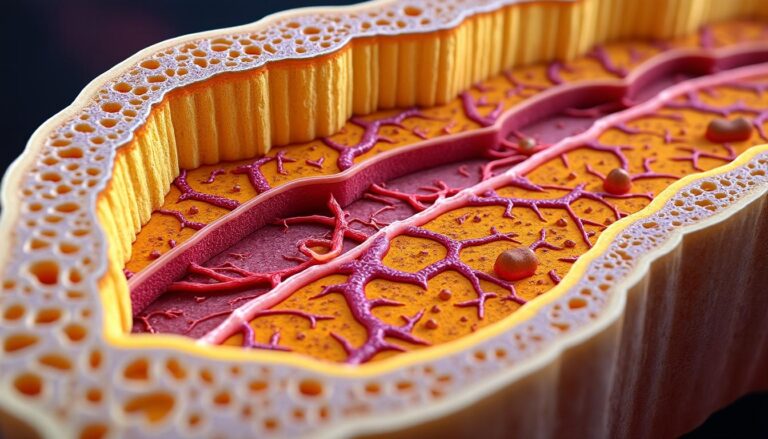
Au cœur de nos os vit un organe discret mais décisif pour l’équilibre de l’organisme : la moelle osseuse. Elle fabrique, renouvelle et oriente les cellules du sang, tout en entretenant une mémoire immunitaire qui nous protège durablement. Ce tissu, à la fois conjonctif et hautement vascularisé, abrite des cellules souches capables de donner naissance à toutes les lignées hématopoïétiques. Comprendre son architecture, son microenvironnement médullaire et ses boucles de régulation, c’est saisir comment la production de cellules sanguines s’adapte chaque jour à nos besoins : effort, stress, altitude, infection ou hémorragie. Pour rendre ces notions concrètes, suivons Claire, jeune interne en hématologie et coureuse de trail, qui voit défiler au service des cas d’anémie ferriprive après don du sang, des neutropénies post-infectieuses et des thrombopénies médicamenteuses. À chaque fois, la question est la même : la niche médullaire reçoit-elle le bon signal ? Et répond-elle par la bonne différenciation cellulaire ? Quand tout fonctionne, rien ne se voit ; quand la mécanique se dérègle, la fatigue, la pâleur, les infections ou les saignements deviennent les messagers silencieux. Objectif ici : décoder les fonctions biologiques majeures de ce “laboratoire” interne, pour comprendre le rôle immunitaire, la logistique d’export vers le système circulatoire et les signes d’alerte qui imposent d’agir vite et bien.
Moelle osseuse : anatomie, localisation et structure histologique
La moelle osseuse occupe les cavités internes des os plats (sternum, côtes, bassin, vertèbres) et l’extrémité des os longs. Elle se compose d’un réseau de tissu conjonctif réticulé, de sinusoïdes vasculaires et d’un stroma cellulaire (cellules mésenchymateuses, endothéliales, ostéoblastiques) qui constituent le microenvironnement médullaire. Ce dernier agit comme une “tour de contrôle”, délivrant facteurs de croissance et signaux d’adhérence qui orientent l’ancrage, la quiescence ou la migration des cellules souches hématopoïétiques.
Avant de plonger dans les détails, répondez à cette question rapide :
On y distingue deux compartiments fonctionnels : la moelle dite “rouge”, riche en tissu hématopoïétique actif, et la moelle “jaune”, plus adipeuse. À la naissance, l’os est quasi entièrement rempli par la forme rouge, puis l’adiposité progresse avec l’âge dans les diaphyses des membres. Cette répartition n’est pas figée : lors d’une fonction biologique exigeante (anémie aiguë, saignement, infection sévère), la moelle jaune peut partiellement redevenir rouge pour accélérer la production de cellules sanguines. En filigrane, les capillaires sinusoïdes relient la niche au système circulatoire, autorisant la sortie contrôlée des cellules matures.
Moelle rouge vs moelle jaune : composition, localisation et dynamique
La moelle rouge renferme environ 60 % de cellules hématopoïétiques et 40 % d’adipocytes, tandis que la jaune est essentiellement adipocytaire. Chez l’adulte, la forme active se concentre dans le rachis, le bassin, le sternum et les côtes ; la forme jaune domine dans les os longs. Après une hémorragie, Claire observe souvent une réticulocytose : signe que la moelle a relancé la chaîne d’érythropoïèse pour compenser la perte. Ce basculement illustre la plasticité des niches et l’importance des signaux locaux pour canaliser la différenciation cellulaire.
| Type de moelle | Composition | Rôle principal | Localisation adulte | Flexibilité physiologique |
|---|---|---|---|---|
| Moelle rouge | ~60 % cellules hématopoïétiques, ~40 % adipocytes | Hématopoïèse active, rôle immunitaire | Vertèbres, bassin, sternum, côtes, épiphyses | Augmente après anémie/hémorragie (conversion depuis la jaune) |
| Moelle jaune | Majorité d’adipocytes, stroma conjonctif | Réserve énergétique, soutien structurel | Diaphyses des os longs | Peut redevenir rouge si besoin accru en cellules sanguines |
Pour le clinicien comme pour l’athlète, retenir que la moelle est modulable aide à lire les bilans sanguins dans leur contexte d’effort, de récupération ou de maladie.
Hématopoïèse : de la cellule souche à la production de cellules sanguines
Au centre du dispositif, les cellules souches hématopoïétiques, rares et multipotentes, initient l’hématopoïèse. Guidées par le microenvironnement médullaire, elles s’engagent vers les lignées myéloïdes (érythrocytes, granulocytes, monocytes, mégacaryocytes/plaquettes) et lymphoïdes (B, T, NK). Les durées de vie imposent un renouvellement soutenu : environ 120 jours pour les érythrocytes, 10 jours pour les plaquettes, et 2 à 10 jours pour nombre de leucocytes. L’oxygénation, l’érythropoïétine, le fer, mais aussi la disponibilité en folates et B12 pilotent la cadence.
Claire se souvient d’une étudiante sportive présentant une macrocytose : une carence en folates freinait la production de cellules sanguines. Après correction diététique et supplémentation ciblée appuyée par une compréhension du rôle de la vitamine B9, l’hémogramme s’est normalisé en quelques semaines. Morale : sans substrats ni signaux adaptés, la fonction biologique la mieux programmée cale.
Pourquoi cela compte au quotidien ? Parce que la tolérance à l’entraînement, la résistance aux infections et la cicatrisation dépendent directement de la capacité de la moelle à ajuster la sortie cellulaire. Sans récupération et sans apports, on n’entraîne pas la moelle : on l’épuise.
Rôle immunitaire et mémoire : plasmocytes à longue durée de vie et défense anti-infectieuse
La moelle osseuse n’est pas qu’une usine à globules ; c’est un pivot du rôle immunitaire. Les niches abritent des lymphocytes B différenciés en plasmocytes longue durée, qui sécrètent des anticorps pendant des mois après une infection ou une vaccination. En parallèle, la granulopoïèse et la monocytopoïèse fournissent neutrophiles et monocytes, première ligne face aux agents pathogènes.
Clinique à l’appui : après un épisode infectieux hivernal, Claire note souvent une neutrophilie transitoire, reflet d’une moelle qui accélère la sortie via les sinusoïdes. À l’inverse, certains médicaments peuvent induire une neutropénie ; le service adapte alors l’exposition aux risques et surveille étroitement les paramètres immunitaires. Dernier point clé : la mémoire humorale logée en partie dans la niche médullaire explique la persistance d’anticorps protecteurs bien après la disparition des symptômes. La défense est efficace quand la niche reste stable et bien nourrie.
Moelle et système circulatoire : portes de sortie, signaux et chronobiologie
Les sinusoïdes médullaires jouent le rôle d’écluses vers le système circulatoire. Les cellules matures, après différenciation cellulaire, modulent leurs intégrines et récepteurs aux chimiokines pour franchir l’endothélium. Des rythmes circadiens influencent même la libération : la nuit, certaines populations mobilisent davantage, en résonance avec les variations hormonales et nerveuses autonomes.
Sur le terrain, cela se traduit par des numérations variables selon l’heure du prélèvement, l’altitude ou l’intensité récente d’exercice. Demande-t-on trop vite à la moelle ? Claire recommande d’interpréter une NFS avec son contexte (fatigue, perte de poids, infections) et la dynamique sur quelques semaines plutôt qu’un cliché isolé. Une sortie harmonieuse vers le sang reste le meilleur marqueur d’un organe médullaire qui “respire” juste.
Clinique et prévention : quand la moelle envoie des signaux d’alerte
Fatigue inhabituelle, essoufflement à l’effort, infections à répétition, hématomes faciles : autant de drapeaux qui suggèrent un déséquilibre de la fonction biologique médullaire. Les tableaux typiques : anémie carentielle (apports/absorptions), leucopénie post-infectieuse, thrombopénie médicamenteuse. Chez une patiente opérée de la colonne, Claire a vu une anémie post-opératoire se corriger grâce à une prise en charge intégrée : bilan carentiel, nutrition, temps de récupération et relance progressive de l’activité, preuve que le contexte musculo-squelettique et médullaire s’entrecroisent.
Parce que la moelle loge notamment au sein des vertèbres, s’intéresser à la santé rachidienne a du sens. Pour comprendre comment certaines chirurgies modernisent la prise en charge des pathologies du dos, voir ces ressources sur les approches du canal lombaire étroit et les solutions pour un canal cervical rétréci. Dans le même esprit d’hygiène biologique, veiller à l’apport en folates reste un pilier ; ce rappel sur la vitamine B9 et ses fonctions montre pourquoi la production de cellules sanguines dépend autant des signaux que des substrats. En résumé : écouter les symptômes, contextualiser les analyses et corriger les causes, c’est protéger la “fabrique” la plus active du corps.
Vérifiez votre compréhension